当儿科医生卡里·纳多(Kari Nadeau)和我离开加利福尼亚州的帕切科山口(Pacheco Pass)向东行驶时,湾区的丘陵地带变成了绵延的果园和平坦的农田。纳多解释说,在车里待了三个小时后,弗雷斯诺大都市的崎岖轮廓在晴朗的天空下显得格外清晰——但这仅仅是因为冷空气将朦胧的灰色烟雾推到了地平线以下。她话说到一半停了下来,因为我们前面的卡车咳出了一团黑烟。“你看到了吗?”她说,眼睛睁大,声音因惊叹和厌恶而提高。
纳多专门研究哮喘,她正前往弗雷斯诺与参与圣华金儿童健康与空气污染研究的其他研究人员会面。她大约每三个月去一次。在帕洛阿尔托,她与丈夫和五个孩子住在一个通风良好的两层楼的家里,她每周在斯坦福大学的露西尔·帕卡德儿童医院(Lucile Packard Children's Hospital)看几次哮喘病人。大多数孩子住在帕洛阿尔托,但也有少数孩子从弗雷斯诺赶来寻求他们在家乡无法得到的治疗。
那天下午早些时候,当我们靠近城市郊区时,一队队拖着沾满烟灰的拖车的重型卡车隆隆驶过。不远处,面带灰尘的移民工人及其家人,以及无家可归的人,生活在广阔的贫民窟——一排排帐篷、手推车、沙发和自行车散落在各处。尽管弗雷斯诺县是全国最富饶的农业区,但2010年它的贫困率在加利福尼亚州最高,近100万居民中有26.8%生活在贫困中。弗雷斯诺-马德拉(Fresno-Madera)被列为全国颗粒物污染(或烟灰)暴露水平最高的都市区。
帕洛阿尔托和弗雷斯诺简直是两个不同的世界。纳多还在她的病人的肺部和基因中发现了极端的差异。她发现弗雷斯诺的孩子更容易患上哮喘,不是因为肺部损伤,而是因为仅仅两个基因(可能更多)表面的变化改变了他们肺部的工作方式。
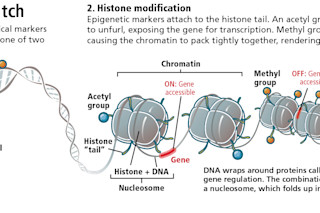
这两个基因对于严格控制免疫系统至关重要,以防止其对良性物质做出反应并引发哮喘症状。与突变不同,这些基因表面的变化——表观遗传学的一部分——在不重写它们编码的信息的情况下改变了这些基因的行为方式。这就像给它们贴上便利贴,告诉细胞是打开还是关闭一个基因。纳多发现,在弗雷斯诺的孩子中,长期暴露于空气污染和二手烟会关闭两个特定的基因。帕洛阿尔托的孩子也发生了类似的变化,但发生率显著降低。
纳多认为严重污染会导致引发哮喘的表观遗传学变化,这些变化可能持续一生,甚至跨越几代人。纳多花了数年时间才建立起这种联系。现在的问题是,这一发现是否有一天能导致该疾病的治疗。
呼吸的权利
49岁的纳多对哮喘了如指掌——她从3岁左右就开始与哮喘搏斗。那时,她害怕睡觉。每晚,她都会尽可能地坐直,脸上绑着装有哮喘药物的雾化器,警惕着哮喘发作:那种沉重、灼热的疼痛;那种喘不过气来的恐慌。在新泽西州纽瓦克烟雾弥漫的岸边的一艘船屋上住了几年,这并没有帮助。到了小学,纳多已经接受了呼吸问题作为现实——这种现实一直持续到今天。她知道哮喘发作可能会要她的命。
纳多的哮喘激励她成为一名医生。作为一名本科生,她帮助在尼加拉瓜建立了一家医疗诊所和污水处理系统。这种影响一直伴随着她。在哈佛医学院,她想给其他学生提供同样的机会,在全球范围内保护人们获得医疗保健的权利,于是她启动了大学与“医生促进人权组织”之间的合作。
纳多收到了关于德克萨斯州哈灵根联邦移民拘留中心儿童结核病爆发的报告。儿童感染导致疫情爆发似乎不合逻辑;他们通常没有足够的力量咳出肺部深处的传染性黏液。因此,1994年秋天,她飞往哈灵根。
当纳多进入那座高耸的白色建筑,往营房里一瞥时,她看到孩子们堆在成排的军用双层床上——其中还有引发疫情、被挤出自己住所的成年人。拥挤的环境为结核杆菌创造了完美的滋生地。
“这真的触动了我,”纳多说。“孩子们被置于这种境地。他们完全无法控制。”在她将自己的发现详细发表在《西部医学杂志》上之后,该中心将成年人搬回了他们的设施。她那时意识到作为一名医生,她有能力为那些对自己的环境没有发言权的儿童争取权益。
从哈佛毕业后,纳多在波士顿儿童医院担任儿科血液病和癌症专科住院医师。由于情感上的疲惫,她在一家生物技术公司工作了几年。她离开了企业界,并于2008年在帕卡德儿童医院获得了过敏、哮喘和免疫学研究员职位。
纳多研究了名为调节性T细胞(或T-regs)的免疫细胞。它们听起来就是这样:调节器,阻止另一组细胞,即辅助性T细胞失控增殖。把T-regs想象成警察,严格控制辅助性T细胞“攻击犬”。我们需要辅助性T细胞;它们启动免疫系统以应对潜在入侵者。但是,过多的辅助性T细胞会导致免疫系统过度活跃,引起咳嗽、气道收缩、黏液分泌和其他哮喘症状。
纳多怀疑哮喘患者的T-regs功能不如健康人,于是她从成人和儿童患者的血液样本中分离出T-regs,并测试它们抑制辅助性T细胞的能力。她200名患者中大多数人的“警察”T-regs都能控制辅助性T细胞。但有30人的T-regs功能不佳,导致辅助性T细胞不受控制地增殖。他们也患有更严重的哮喘症状。一个女孩不离开家就会引发哮喘发作,而一个男孩的过敏如此严重,以至于他不得不寻求残疾身份。
纳多持怀疑态度,重复了实验,但同样是那30名患者出现了。他们有相同的种族或社会经济地位吗?不是。她想,这一定是某种环境暴露,也许与他们在帕洛阿尔托的居住地有关。
纳多查看了她的儿科病人的邮政编码。那15个孩子不是来自帕洛阿尔托。他们住在弗雷斯诺,一个她很快就知道空气污染严重(主要是卡车、汽车和拖拉机的柴油废气)的城市,这与帕洛阿尔托的晴空形成了鲜明对比。她强烈预感这种污染已经使她的弗雷斯诺病人的T-reg功能失常。

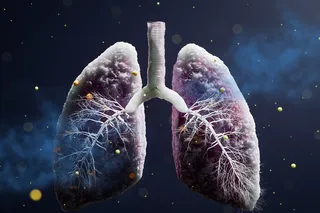
弗雷斯诺的空气中弥漫着烟灰。空气污染似乎会加剧两个基因的功能,这可能导致哮喘症状。| ZUMA Press Inc./Alamy
但她的样本量仍然很小,以至于她不能排除统计上的巧合。因此,2008年,她直接打电话给伊拉·塔格(Ira Tager),一位现已退休的加州大学伯克利分校环境流行病学家,向他报告了她的发现。在过去的十年里,塔格一直在弗雷斯诺进行一项大规模研究,考察污染如何影响肺部。
他觉得纳多的研究结果很有意思,并邀请她到伯克利拜访他。两人一拍即合,他同意让纳多采集他弗雷斯诺受试者的血液,以检查污染是否也使他们的T-reg功能恶化。
作为纳多和塔格研究的一部分,参与者填写了关于他们接触污染和二手烟的问卷。空气质量监测和统计模型测量了每个人的污染暴露情况。
现在纳多有了更大的患者群,包括弗雷斯诺和帕洛阿尔托患有和未患哮喘的儿童。她发现帕洛阿尔托未患哮喘的儿童的T-reg功能最好。即使是帕洛阿尔托患有哮喘的儿童,其T-reg功能也比弗雷斯诺未患哮喘的儿童好。当然,弗雷斯诺患有哮喘的儿童的T-reg功能最差。
为了弄清其机制,纳多关注了基因*Foxp3*,该基因能促使未成熟的T细胞发育成那些“警察”细胞,即T-regs。研究表明,缺乏*Foxp3*的儿童会患上哮喘、过敏和自身免疫性疾病。纳多偶然发现了一项小鼠研究,该研究描述了环境因素如何用化学标记标记*Foxp3*,这些标记告诉T细胞前体打开或关闭该基因。用甲基基团标记Foxp3就像在其上贴上写着“关闭”的便签。乙酰基团的便签写着“开启”。
“那篇论文改变了我的生活,”纳多说。“如果这发生在小鼠身上,那么很可能也发生在人类身上。”一些研究还表明,这些表观遗传学变化是可以遗传的。
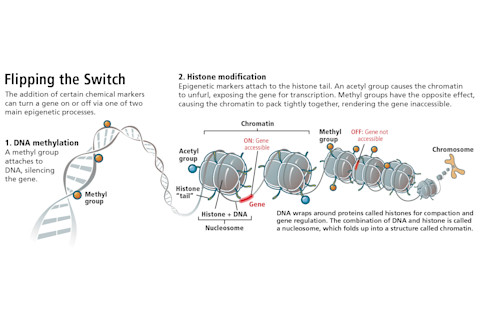
杰伊·史密斯
一旦纳多理解了甲基基团在基因表达中的作用,所有的点就都连接起来了。她认为,空气污染通过用甲基基团标记未成熟T细胞中的Foxp3,关闭其表达,从而在她的弗雷斯诺患者中引发哮喘。这阻止了细胞成熟为那些控制辅助性T细胞的“警察”T-regs。因此,更多的污染暴露意味着更多的甲基基团。
结果显示,帕洛阿尔托没有哮喘的儿童,其*Foxp3*基因的甲基化程度最少;而患有哮喘的帕洛阿尔托儿童,甲基化程度更高。在弗雷斯诺没有哮喘的儿童中(他们在更多污染的环境中长大),该基因的甲基化程度更高。而弗雷斯诺患有哮喘的儿童,*Foxp3*基因的甲基化程度最高。“只有一个分子如此突出,这似乎令人惊讶,”纳多说。
纳多和塔格于2010年在《过敏与临床免疫学杂志》上发表了他们的研究结果。与此同时,哥伦比亚大学、辛辛那提大学和其他机构的研究人员也开始发表类似发现。但这一趋势令人担忧:污染的印记并非弗雷斯诺独有。科学家们在全国各地的污染城市都看到了同样的影响。
烟幕
纳多的发现揭示了污染可以通过从根本上改变我们的生物学,改变我们基因的行为方式来导致哮喘。2010年的论文发表后,她想,二手烟是否也有类似的效果?它也可能导致哮喘,而且研究表明,儿童,特别是生活在弗雷斯诺等贫困社区的儿童,特别容易受到二手烟的影响。纳多想弄清楚暴露于二手烟如何影响甲基化和基因表达。科学家们已经发现吸烟会导致表观遗传学变化。但这些变化是什么?它们又是如何引发哮喘的呢?
在纳多诊所的一间小办公室里,她实验室的本科生阿鲁尼玛·科利正在梳理纳多和塔格收集的问卷和污染数据。由于问卷询问了参与者接触二手烟的情况,纳多要求科利将这些答复纳入他们免疫细胞的分析中。“这就在我们手边,”纳多想。
纳多想研究空气污染和二手烟(两者都与哮喘有关)如何促使Foxp3发生表观遗传学变化。如果这些压力源表观遗传学地改变了Foxp3,那么它们可能也影响了其他调节过敏途径的基因。由于研究表明,中央谷地重度污染地区的儿童感染率更高,而且污染和二手烟含有相似的有毒化合物,纳多便寻找在对抗感染中起重要作用的基因。了解它们如何工作可能有助于指明治疗它们的方法。她还寻找控制辅助性T细胞成熟开关的基因,以维持辅助性T细胞的恰当平衡——在抑制过敏反应的Th1细胞和引发过敏反应的Th2细胞之间。
纳多最终锁定了蛋白质编码基因干扰素γ,它不仅在对抗感染中很重要,而且在维持辅助性T细胞的微妙平衡中也发挥作用。当干扰素γ被甲基基团覆盖——或被关闭——它会打破平衡,刺激Th2细胞的发展,并使免疫系统过度活跃。
纳多怀疑弗雷斯诺的孩子们受到了Th2细胞的双重打击。他们不仅干扰素伽马表达水平低,而且Foxp3表达水平也低,这意味着他们更少的T-reg细胞来管理辅助性T细胞。纳多怀疑弗雷斯诺儿童体内充满了引发哮喘的Th2细胞。
这意味着污染和二手烟可能具有协同效应。为了验证这一点,科利绘制了每个孩子接触污染和二手烟的程度与Foxp3和干扰素γ的甲基化和表达水平的关系图。
渐渐地,一幅画面浮现出来。这两个基因的最高甲基化和最低表达出现在同时接触二手烟和污染的弗雷斯诺患者中。但在纳多兴奋之前,她需要重复分析;她需要确定。她把数据交给了塔格、一位统计学家和另一个实验室。每个人都计算出了相同的结果。
“然后我们才知道,天哪,这真的发生了,”纳多说。
多年来,研究表明污染会导致哮喘,而且这种疾病往往在家族中发生。现在,纳多和科利的研究结果于2012年秋季发表在《临床表观遗传学》上,提出了一种潜在的机制。他们还将烟草烟雾的两种影响——甲基化和哮喘——联系起来,表明烟雾引起的表观遗传学变化也可能导致哮喘。
家族遗传
然而,污染和二手烟留下的分子疤痕可能不会止步于受其影响的人。研究表明,它们可以遗传给子孙后代,这意味着可能需要几代人才能看到其全部影响。2012年发表在《生物医学中心医学》上的一项研究发现,暴露于尼古丁的怀孕大鼠的后代和孙辈都患上了哮喘,即使这些后代没有接触过这种化学物质。
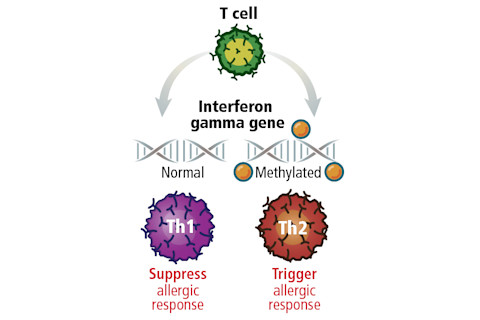
甲基化关闭基因,扰乱T辅助细胞的平衡。| 杰伊·史密斯
纳多给了一个人类的比喻。想象一位母亲在她年幼的女儿身边吸烟,导致她女儿身上发生表观遗传学变化,这种变化一直持续到成年,即使她搬走了。当她有了自己的孩子时,“那个孙子将拥有祖母因为吸烟而产生的同样的表观遗传学变化,”纳多说。
但与基因突变不同,我们可以“撤销”不良的表观遗传修饰。我们对个体易感性或弹性机制的理解越深入,研究人员就越能设计出有效的干预措施。纳多的团队正在努力识别T-reg通路中的信号蛋白,并开发一种筛查方法,通过测量各种生物标志物(包括Foxp3和干扰素γ表达)的比例来预测过敏和哮喘的预后。他们另一项研究的初步数据表明,弗雷斯诺的年轻人通过搬到其他地方上大学,他们的免疫细胞的一些表观遗传学变化可能会逆转。到目前为止,这些细胞的表观遗传学变化已持续了一年。“但我们仍将长期测试这一点,”纳多说。
一些生物伦理学家怀疑,即使是最令人信服的关于污染跨代影响的研究,也无法说服立法者实施进一步的改革。“我们对地球或我们子孙后代并非特别好的管理者,”路易斯维尔大学医学院的生物伦理学家马克·罗斯坦说。
尽管如此,就像父母在孩子受苦时会尽一切努力一样,纳多也无法袖手旁观,因为她知道自己的工作有机会帮助孩子们克服因偶然而非选择导致的诊断。“孩子们不应该受苦,”她说。“我们需要比我小时候更好的药物,而且在达到目标之前我不会停止。没有人应该眼睁睁看着自己的孩子死去。”
[本文最初以“空气中的某种东西”为题刊登在纸质版上。]