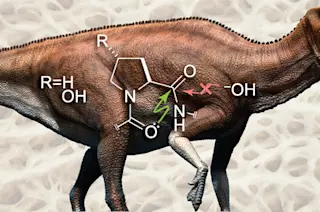
胶原蛋白是动物体内含量最丰富的蛋白质。它也是最持久的蛋白质之一。在过去几十年里,古生物学家在数千万年前的恐龙化石中发现了它。
它的持久性令人费解,因为该蛋白质含有的化学键,理论上应该只能持续 500 年。那么,为什么这种物质能保存如此之久呢?化学家在《ACS Central Science》的一篇报道中对此谜团给出了答案。
胶原蛋白的强度
答案始于胶原蛋白的结构。胶原蛋白由三条蛋白质链组成,它们缠绕在一起,形成一种比单独一条链子强得多的物质。
“胶原蛋白链形成三重螺旋,”麻省理工学院的化学家、该论文的作者之一Ron Raines说。“三重螺旋是一种非凡的结构,它至少在 2 亿年来一直作为动物身体的支架。我想知道,胶原蛋白三重螺旋的进化是否促进了大约 10 亿年前地球上生命的出现!”
然而,即使是最强的绳索也会随着时间的推移而磨损、起毛、最终断裂。那么,为什么胶原蛋白不会呢?
阅读更多:对骨骼的新分析有助于解释其为何如此坚固
胶原蛋白如何抵抗水
这就是胶原蛋白长寿之谜的核心。氨基酸——构成胶原蛋白链的组成部分——在接触水时通常会分解,就像普通绳子会被雨水侵蚀一样。出于某种原因,连接胶原蛋白中氨基酸的肽键(本质上是连接链条的化学“胶水”)在潮湿时不会分解。
为了研究原因,化学家设计并合成了小分子,使他们能够测试这些小分子如何与胶原蛋白中相邻的肽键发生反应。
“本质上,我们可以‘开启’或‘关闭’这种相互作用,然后观察结果,”Raines 说。他们尤其关注观察水解——水分解化学物质的过程。
“我们发现,‘开启’这种相互作用可以阻止水解,”Raines 说。
阅读更多:石化的恐龙蛋壳可以在数百万年间保存氨基酸
电子共享和泡利不相容原理
其原理有些深奥,因为它涉及到一种称为“泡利不相容原理”的量子力学效应。
该原理指出,分子中的一个轨道最多可以容纳两个电子,不能更多。由于胶原蛋白的组成部分在整个结构中共享电子,因此水分子中的电子几乎没有空间来干扰这些化学键。
“胶原蛋白在整个结构中允许这种相邻电子共享方面是独一无二的,”Raines 说。“没有其他蛋白质能像这样免受水解的侵害。”
那么,我们现在知道了为什么我们富含胶原蛋白的骨骼和软骨如此坚韧,科学家们又能用这些信息做什么呢?研究人员已经展示了如何工程化类似的化学键,使其易受水的影响——包括用于可生物降解的餐具。
“相关的应用当然是可能的!”Raines 说。
阅读更多:首次观察到泡利量子晶体
文章来源
我们的Discovermagazine.com作家在文章中采用同行评审研究和高质量来源,我们的编辑会审阅科学准确性和编辑标准。请查看本文使用的以下来源
《ACS Central Science》。n→π* 相互作用的泡利不相容原理:对古生物学的启示
麻省理工学院化学家。Ron Raines
在加入Discover Magazine之前,Paul做了20多年的科学记者,专注于美国生命科学政策和全球科学职业问题。他的职业生涯始于报纸,后来转向科学杂志。他的作品曾出现在《科学新闻》、《科学》、《自然》和《科学美国人》等出版物上。