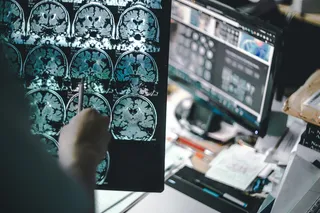
Elijah Stommel是新罕布什尔州达特茅斯-希区柯克医疗中心的一位神经科医生,他经常不得不向病人传达坏消息,但他尤其害怕一种诊断结果。
肌萎缩侧索硬化症,或称ALS,会杀死大脑和脊髓中的运动神经元,逐渐使身体瘫痪,直到吞咽和呼吸都变得不可能。ALS的病因不明。尽管对患者来说几乎没有安慰,但Stommel过去常常提供一个令人安慰的事实:ALS很罕见,每年随机袭击十万人中的两人。
几年前,为了更深入地了解这种疾病,Stommel请学生们将他大约200名ALS患者的街道地址输入Google Earth。
什么是BMAA?
新英格兰电脑生成地图上出现的病例分布让他震惊。他的现有患者和已故患者的家集中在湖泊和其他水体周围,其数量远远高于国家统计数据的预测。
标记他们位置的密密麻麻的点在风景如画的马斯科马湖周围最为密集,那是一个距离达特茅斯医学院仅10英里的乡村地区。那里出现了大约十几个病例,其中大多数是在过去十年内诊断出来的。这种模式看起来根本不是随机的。“我开始想,水里可能有什么东西,”Stommel说。
他现在怀疑,“那种东西”可能是环境毒素β-甲基氨基-L-丙氨酸,或称BMAA。这种化合物由蓝细菌(生活在土壤、湖泊和海洋中的蓝绿藻)产生。
蓝绿藻毒性
蓝细菌被鱼类和其他水生生物食用。最近的研究在海鲜中发现了BMAA,这表明某些饮食和地点可能使人们面临特殊风险。更令人担忧的是,蓝细菌水华变得越来越常见,这加剧了人们的担忧,即它们的有毒副产品可能正在悄然助长ALS的激增,以及阿尔茨海默病和帕金森病等其他神经系统疾病的发生。
情况如此严峻,以至于来自11个国家的21个研究团队现在正在调查BMAA的潜在危险。“有一个团队强烈否认了这一假设,”迈阿密大学米勒医学院神经科医生、ALS主要权威Walter Bradley说。“但越来越多的科学家意识到这是一个可行的假设,关于这个话题的论文正在像滚雪球一样增多。”
BMAA毒素的潜在危险
关于BMAA潜在健康威胁的线索可以追溯到半个世纪前的遥远太平洋岛屿关岛。在那里,二战结束后,美国陆军医生遇到了一种奇怪综合征的爆发,当地人称之为lytico-bodig——其中lytico意为瘫痪,bodig意为痴呆。
一些受害者有类似ALS的症状,另一些则表现出帕金森病的僵硬姿势,还有一些则表现出阿尔茨海默病典型的精神模糊。
一个由梅奥诊所神经学家Leonard Kurland领导的美国团队确定,lytico-bodig的最高发病率发生在乌马塔克(Umatac),一个位于关岛南部海岸的茅草屋顶小村庄。
阅读更多:压力会导致认知能力下降吗?
关岛的Lytico-Bodig疫情爆发
在1950年代疫情高峰期,村里几乎家家户户都至少有一名患者。岛上的原住民查莫罗人受到严重影响。移居关岛并采纳当地习俗的菲律宾人也以高比率患上这种疾病,但通常只有在岛上生活至少10年才会被感染。这种模式表明,这是一种潜伏期很长的感染,或者是一种随着时间积累的毒素。
世界各地的医学研究人员纷纷涌向关岛,希望通过lytico-bodig来揭开神经退行性疾病更广泛的奥秘。他们很快就集中精力研究乌马塔克饮食中一种独特的成分,一种名为苏铁的原始棕榈状植物,查莫罗人将其种子磨成面粉制成玉米饼。也许是苏铁中的某种化合物是罪魁祸首。
分析BMAA
在1960年代,英国生物化学家Arthur Bell、Peter Nunn和Armando Vega在伦敦国王学院分析了苏铁种子,并重点研究了其中的一种化合物BMAA。吸引他们注意的是其分子结构:BMAA类似于β-草酰氨基-L-丙氨酸(BOAA),这是一种在亚洲鹰嘴豆中发现的物质,已知会引起一种麻痹性疾病。
试管实验表明,BMAA可以杀死脊髓中的运动神经细胞,正是ALS所破坏的那些细胞。更多的证据来自一项对喂食高剂量该化合物的猴子的研究。猴子开始行动迟缓并颤抖,它们的脸上出现了一种僵硬的表情,这反映了lytico-bodig的一些症状。此外,尸检结果显示,这些动物的大脑也受到了运动神经元的损伤。
这些发现最初燃起了科学界捕获一种破坏大脑的杀手的希望。然而,其他研究人员提出了质疑。美国国立卫生研究院神经科学家Mark Duncan指出,需要巨量剂量的BMAA才能在猴子身上产生症状。
他计算出,一个查莫罗人每月需要吃将近一吨苏铁粉才能获得等量的剂量。在关岛,这种毒素怎么可能以如此高的含量被摄入,这是不可思议的。没有发现其他合理的lytico-bodig病因。到1990年代初,疫情正在消退,线索也中断了。
阅读更多:确定痴呆症是否是人类独有的
考艾岛果蝠和苏铁种子
就在研究似乎陷入僵局的时候,考艾岛夏威夷国家热带植物园当时的园长Paul Cox重新提出了这个问题。作为他在那里的研究的一部分,Cox研究了蝙蝠,这项工作让他灵光一闪。他注意到关岛的查莫罗人喜欢吃当地的一种果蝠,以至于到1980年代后期,这种动物被捕杀到几乎灭绝。
考克斯对这些蝙蝠的饮食很感兴趣:它们以苏铁种子为食。他提出BMAA在蝙蝠体内浓缩,或者说生物放大,其含量比在苏铁粉中发现的要高出许多倍。他假设,对于那些经常吃果蝠的人来说,累积的BMAA剂量可能足以对大脑造成损害。此外,关岛果蝠(特别是被称为飞狐的那种)的日益稀缺可能解释了lytico-bodig爆发为何逐渐平息。
Cox以发现抗艾滋病药物原丁蛋白(prostratin)而闻名,该药物提取自萨摩亚的mamala树,他在民族植物学领域备受尊敬,但关岛疫情的老兵们认为他是一个新手,不可能在神经科学巨擘失败的地方取得成功。但这并没有阻止他尝试。在加州州立大学富勒顿分校的太平洋蝙蝠专家Sandra Banack的帮助下,Cox测试了1950年代疫情高峰期在关岛采集的三份果蝠标本。2003年,他们发表了研究结果。所有的蝙蝠都富含BMAA。
BMAA、Lytico-Bodig和阿尔茨海默病之间的联系
Cox随后着手获取六名死于lytico-bodig的查莫罗人在尸检期间收集的脑组织样本。他将这些样本与从15名加拿大人(其中两人死于阿尔茨海默病,13人在死亡前没有神经病理学迹象)身上提取的脑组织进行比较。
他联系了多伦多病童医院的生物化学家、人体组织中生物分子发现专家Susan Murch,以进行双盲研究测试样本。六个查莫罗人的大脑都含有BMAA。令人震惊的是,加拿大两名阿尔茨海默病患者的大脑也含有BMAA,而13个对照组则一点都没有。“突然间,这不再是一个关于一个小岛上偏远民族的故事,”Cox说。
此时,Cox面临着一个新的谜团:BMAA是如何进入远离关岛的阿尔茨海默病患者大脑的?当他追溯苏铁种子中BMAA的来源是生长在植物根部的蓝细菌时,答案就来了。产生这种有毒化学物质的不是植物,而是与之相关的微生物。Cox总结道,BMAA的影响范围远远超出了关岛的苏铁树。
阅读更多:痴呆症的4种主要类型
鱼类和软体动物中的蓝细菌
蓝细菌是地球上最普遍的生物之一。它们通常存在于土壤中,但也存在于水中,在那里微生物形成水华,常见于河流和湖泊表面粘滑的绿色薄膜。
蓝细菌是水生食物链的基础,是鱼类和软体动物最喜欢的食物,而这些又被我们食用。
当考克斯思索蓝细菌在地球食物网中的核心作用时,他说:“那一刻,我感觉自己仿佛凝视着深渊。”
揭露BMAA危害的圣战
如今,作为怀俄明州杰克逊霍尔民族医学研究所的所长,考克斯正独自一人致力于将科学的聚光灯投向BMAA的危险。当我第一次在2009年迈阿密大学举行的一次关于该主题的研讨会上见到他时,他的努力已经催生了一个名副其实的“家庭手工业”:来自世界各地约50位BMAA研究人员聚集在那里,每个人都带来了谜题的不同部分。
考克斯是一位五十多岁的大个子,一头乌黑的头发夹杂着灰白,他讲话生动而平易近人。他将BMAA描述为一个“分子不速之客”。他解释说,它是一种氨基酸,是我们细胞中构成所有蛋白质的20种分子的化学亲戚。大多数人的身体可以代谢或排出这种化学入侵者,但某些有遗传易感性的人可能无法做到。
当他们食用被BMAA污染的食物或饮料——无论是炖蝙蝠、贝类还是受污染的水——这种分子都不会被排出;相反,它会被吸收并沉积在大脑中,形成Cox所谓的“毒素储存库”。他说,一旦进入大脑,“BMAA就会被整合到蛋白质中,可能导致它们截断甚至崩溃。”他认为,这就是它引发神经功能障碍和阿尔茨海默病等疾病的原因。
支持考克斯理论的研究:追踪啮齿动物体内的BMAA
在听了Cox的理论后,迈阿密大学脑捐赠银行的负责人、神经科学家Deborah Mash确信他有所发现。Mash是一位身材娇小、波浪状棕色头发和锐利绿眼睛的女士,她对BMAA的激情似乎不亚于Cox本人。
在大学市中心医疗园区的一栋矮红砖建筑的实验室里,她描述了她的团队如何将放射性标记附加到BMAA上,将其注射到啮齿动物体内并进行追踪。她的结果似乎证实了Cox的解释。
“BMAA会被大脑吸收,然后其含量趋于稳定,这表明它正在被整合到蛋白质中——它被困住了,”她说。“这听起来确实像一个毒素储存库。”
人脑中的BMAA:阿尔茨海默病和ALS的关联
在Cox的敦促下,Mash着手利用她自己的人类脑库样本,对ALS和阿尔茨海默病大脑进行一项独立研究。这些样本中的许多来自一生大部分时间都在佛罗里达州以外度过的捐赠者,因此他们一生中接触BMAA的程度可能差异很大。
为了进行一项有意义的实验,Mash希望精确复制Cox的方法,因此她派了一位同事,神经科学家John Pablo,到杰克逊霍尔的实验室。在那里,Pablo学习了Cox区分BMAA和类似天然氨基酸的技术——一种仍然引起争议的方法。掌握了细节后,Pablo返回进行测试。
结果是显著的。迈阿密团队在12名阿尔茨海默病患者的24份样本中发现了BMAA,但在12名对照组的24份样本中只发现了2份。他们还测试了13名ALS患者的样本,所有样本的BMAA检测结果均呈阳性。
为了探究这种化学物质是否是任何导致神经元死亡的疾病的结果,而非特定原因,Mash和Pablo进行了另一项实验。他们测试了死于亨廷顿病(一种脑基部神经细胞退行性疾病)的人的神经组织。亨廷顿病已知是纯粹的遗传病。这次的结果看起来非常不同。在来自八个人的16份样本中,几乎没有BMAA的痕迹。
影响BMAA诱发疾病的因素
Mash推测,一个人是否会因神经毒素而生病,可能取决于许多因素。这些因素包括终生暴露的剂量以及影响BMAA是否被肠道吸收、被肝脏破坏或被允许穿过血脑屏障的个体生物化学差异。“还需要弄清楚更多的谜团,”她说,“但显然,对人类健康的潜在影响可能是巨大的。”
2006年,迈阿密大学罗森斯蒂尔海洋与大气科学学院的浮游植物专家、Mash的同事Larry Brand开始收集更多针对BMAA的证据。Brand在过去15年里花了很多时间在海上研究蓝细菌水华。“当Paul Cox发表论文称蓝细菌产生BMAA时,”他带着浓重的德克萨斯口音说,“我想,哇,我们最好调查一下,因为在佛罗里达这里我们有一些非常大的水华。”
他报告称,全球范围内,蓝细菌和藻类水华的发生频率更高,覆盖淡水和海水区域也更大。微生物在温暖的水域中繁殖更快,并依赖污水和农业径流生长。他推断,如果鱼类食用更多的蓝细菌并在体内积累更多的BMAA,那么对人类健康的负面影响很可能会加剧。
蓝细菌水华和BMAA的全球影响
Brand正试图通过追踪BMAA在佛罗里达州定期发生蓝细菌水华的水域食物链中的流动情况来了解这种风险。他送往Mash实验室的许多鱼类和贝类样本不含BMAA,但也有不少样本含有BMAA。底栖生物的含量明显较高,这可能是因为蓝细菌不仅在海面,而且在海底也会积累。
与关岛果蝠中发现的BMAA含量相比,布兰德在佛罗里达牡蛎和贻贝中发现的毒素含量适中。但粉虾、大口鲈鱼和蓝蟹——这些都是人类食用的——所含的毒素水平与蝙蝠相当,甚至超过蝙蝠。一只蓝蟹的BMAA含量高达7,000 ppm,是关岛蝙蝠中毒素含量的两倍。
“这真是个震惊的消息,”布兰德说。他想知道这是否是一个偶然事件,但他的团队从切萨皮克湾水华区采集的蓝蟹也含有同样高水平的BMAA。去年,瑞典研究人员还在波罗的海的底栖鱼类中发现了这种神经毒素,波罗的海是蓝细菌水华的热点地区,尽管其含量低于切萨皮克湾和佛罗里达沿海地区。
阅读更多:为什么一大片海藻正向佛罗里达漂来?
围绕BMAA理论的争论与质疑
BMAA与神经系统疾病之间的关联似乎很强——但正如怀疑论者指出的那样,关联并不能证明因果关系。这只是他们对考克斯理论的一个问题。
该领域一直受到相互矛盾的发现的困扰,导致一些批评者质疑BMAA是否真的是一种强效神经毒素。“你可以给小鼠喂食任意多的BMAA,但在大脑中根本看不到它,”不列颠哥伦比亚大学温哥华分校神经科学家Christopher Shaw说。此外,他表示,目前没有已知的机制可以解释一种对人类生物学陌生的氨基酸如何能够穿过血脑屏障,被整合到蛋白质中,然后逐渐导致疾病。
更令人怀疑的是,由加州大学圣地亚哥分校阿尔茨海默病研究中心主任Douglas Galasko领导的团队两次试图在死于脑部疾病的查莫罗人和北美洲人身上找到BMAA——两次都一无所获,尽管他们使用的化学识别方法与考克斯和迈阿密团队所用的不同。
亚特兰大疾病控制与预防中心的神经学家兼流行病学家David Thurman补充说,即使BMAA确实像Cox所认为的那样起作用,它也不太可能成为ALS和阿尔茨海默病等神经系统疾病的主要因素。他指出,大多数专家认为这些脑部疾病有多种病因,包括基因、不良饮食、缺乏运动以及各种环境因素,包括病原体和杀虫剂。
Paul Cox对BMAA风险的务实看法
令人惊讶的是,Cox同意BMAA的总体风险可能很低。事实上,他津津有味地吃虾和螃蟹。“ALS非常罕见,只有少数人有遗传风险,”他说。“即使BMAA导致阿尔茨海默病和帕金森病等常见疾病,这仍然不意味着我们应该避免食用海鲜。”
他指出,商业渔民通常不在蓝细菌严重污染的区域作业,因此对于那些食用典型的商店购买或自家种植的食物并避免饮用——正如考克斯所说——“绿色、有臭味”的水的人来说,在美国和加拿大接触到这种危险的风险应该很小。
阅读更多:全球渔业资源下降的真正原因——以及你能为此做些什么
持续研究:调查ALS群集
尽管如此,考克斯和他的同事们仍在继续努力,原因与1950年代研究人员蜂拥至关岛的原因相同:如果BMAA暴露至少导致了一些最严重的神经系统疾病,那么更多地了解这种模糊的化合物可能对理解潜在疾病具有巨大意义。
最近,考克斯和同事们一直在研究日本东南纪伊半岛的ALS病例群,他还与迈阿密大学神经学家布拉德利联手研究第一次海湾战争美国退伍军人中发病率较高的疾病。
与达特茅斯大学的ALS专家Elijah Stommel合作,Cox还在调查新英格兰地区特有的病例群。随着他们的工作传播开来,更多的医生报告了该地区的病例,ALS患者的数量从Stommel原始数据库中的200人跃升至今天的800人。
BMAA暴露与ALS的联系:地理模式
有时,由于随机波动,某种疾病在一个地点比另一个地点更普遍,因此这两位研究人员正在与流行病学家合作,他们正在使用地理软件程序来区分真正的集群和假象。
数据显示,在蓝细菌水华发生过的湖泊或池塘半英里范围内,ALS的患病率比平均水平高2.5倍。Stommel推测,生活在湖泊周围的人们可能通过空气吸入BMAA,食用了受污染的鱼类,或在游泳时意外吞食了它。他和Cox正在对脑库组织进行测试,以查明这些地区的ALS患者是否确实BMAA水平升高。
历史案例:揭示BMAA暴露随时间的变化
随着证据的积累,Cox已经在思考如何在疾病发生前检测毒素暴露的方法。他回忆起一个引人入胜的案例:一位死于进行性核上性麻痹(一种类似ALS的疾病)的女性。在她去世前几十年,她习惯剪下自己的头发,注明日期,然后放入日记。由于几乎所有摄入的物质都会在头发中留下痕迹,Cox和生物化学家Murch意识到他们有机会查看这位女性是否曾暴露于BMAA。
他们发现,早在1939年,她的头发就开始积累这种毒素,并且在接下来的二十年里,毒素含量逐渐上升。到1957年,这种神经毒素已经达到了Cox在阿尔茨海默病患者身上测得的丰富程度。含量在1962年左右达到峰值,然后开始下降,在她去世时已检测不到。
“如果我们有时间机器,”考克斯思考道,“我们可以在1957年回到过去,取一个头发样本,然后告诉她,‘你正在积累一种非常奇怪的神经毒素。’我们就会发现她是如何接触到的,并可能预防她的疾病。”
未来对BMAA有害影响的检测
将来,医生可能会定期检测BMAA过载。他们甚至可能能够抵消其影响。然而,在卫生官员考虑限制环境暴露于BMAA之前,他们需要更有力的危害证据。为此,Mash希望在灵长类动物身上再次测试这种化合物。“唯一一次进行的猴子试验无疑非常具有启发性,”她说。令她沮丧的是,资助机构一直不愿在一个如此有争议的理论上投入资金。
目前,马什和考克斯抓住每一个线索,希望能找到决定性的证据。在过去的几年里,法国和瑞典的研究人员已经表明,当BMAA注射到啮齿动物体内时,它会进入它们的眼睛(pdf),并在那里积累,可能对视网膜细胞造成损害。近一半死于lytico-bodig的查莫罗人表现出视网膜细胞损伤。
大多数专家将这种损害归因于寄生虫,而不是BMAA。但关岛纪念医院的神经科医生约翰·斯蒂尔,曾主导该疾病的一些关键研究,他补充了一个听起来……可疑的细节:尽管进行了深入研究,但没有人能确定这种寄生虫到底是什么。
阅读更多:我们的水中有PFAS。我们如何去除它们?