杰克·凯鲁亚克,图片来源:汤姆·帕伦博
要点:法裔加拿大人较高的孟德尔疾病发病率可能与其人口历史有关。
正如我之前指出的,对群体遗传变异特征产生极其强烈影响的人口瓶颈,其性质必须非常彻底才能具有任何意义。人口瓶颈必须是数百人,而不是数千人。
但这并不排除更温和的瓶颈效应会在基因位点频率谱中产生微妙的转变
。强烈的瓶颈可能需要推动曾经常见的等位基因完全灭绝(或中等频率的等位基因固定),但温和的瓶颈仍然可能扰乱等位基因频率分布。特别是,以极低频率存在的等位基因数量可能受到人口变异和自然选择的强烈影响。这是作为基于核苷酸序列检测自然选择的测试(例如Tajima's D)的基础的逻辑原理。低频率变异的过度出现表明瓶颈效应和随后的群体扩张,或正向和/或纯化选择。相反,平衡多态性频率指向一个正在缩小的群体或平衡选择。
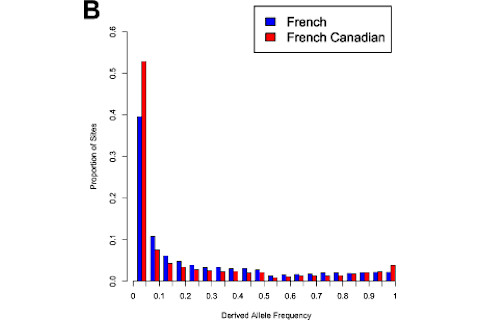
引文:Casals F, Hodgkinson A, Hussin J, Idaghdour Y, Bruat V, et al. (2013) Whole-Exome Sequencing Reveals a Rapid Change in the Frequency of Rare Functional Variants in a Founding Population of Humans. PLoS Genet 9(9): e1003815. doi:10.1371/journal.pgen.1003815
这些基本思想已经存在了几十年,但正是凭借强大的基因组技术,它们才真正为我们提供了可操作的见解。 《公共科学图书馆·遗传学》上的一篇新论文对此做了简单阐述,全外显子组测序揭示了人类创始群体中罕见功能变异频率的快速变化。在左边,您可以看到法国和法裔加拿大人口的位点频率分布。显而易见的是,对于法裔加拿大人的基因组外显子区域的衍生等位基因(即来自祖先状态的突变)分布,其向低频率部分的偏斜程度远大于法国本土人口。这种偏斜对于有害突变,如无义突变和错义突变(无义突变通常产生无功能蛋白,而错义突变可能通过氨基酸替换以某种特定细节改变蛋白的性质),更为明显。
这里的重点是外显子,约占基因组的1%,因为这些区域被翻译成最终的蛋白质产物,作者似乎对法裔加拿大人位点频率谱的功能性后果特别感兴趣。这很合理,因为法裔加拿大人口长期以来一直以隐性疾病负担较高而闻名。为什么?正如论文中所述,法裔加拿大的祖先绝大多数来自一个不到10,000人的创始群体。不仅如此,这个扩张的人口还表现出地理上的亚结构,人口扩张在魁北克定居点边缘尤其强劲。这导致边缘地区的遗传漂变增加,因为人口中较小的一部分对越过边境的后代做出了贡献。关键在于,几百年的人口隔离就可能导致“私有等位基因”的出现,这是多么惊人。在很大程度上,这在直觉上是显而易见的,因为私有等位基因在家族中是从头出现的,许多法裔加拿大家族已经与祖先故土分离了许多代,从而积累了其血统特有的独特标记。
从长远来看,许多“x”全基因组覆盖(因此平均而言,可以通过10、20或30次读取找到相同的碱基,以减少可能的假阳性)将变得无处不在,我们将了解家族内部和家族间的遗传负荷分布。这篇论文强调的一个主要的人口历史动态是,人类历史上的连续瓶颈事件(例如,“走出非洲”迁徙)可能使不同人群具有不同的位点频率谱,从而暗示着不同的遗传疾病负荷。鉴于基因组研究倾向于关注欧洲血统人群,我们尚未深入探讨这些人群间的可能性,但它们即将出现。我怀疑,例如,印度次种姓由于瓶颈效应和近期扩张,往往会有许多私有等位基因。而且,在短期内,这可能也有利于那些主张通过跨人群随机交配实现遗传多样性益处的人。
引文:Casals F, Hodgkinson A, Hussin J, Idaghdour Y, Bruat V, et al. (2013) Whole-Exome Sequencing Reveals a Rapid Change in the Frequency of Rare Functional Variants in a Founding Population of Humans. PLoS Genet 9(9): e1003815. doi:10.1371/journal.pgen.1003815