我们肠道中蠕动的细菌很可能在炎症性肠病、肥胖和其他健康状况中起作用。而我们与互动的人交换细菌。所以也许肠道细菌也能在人与人之间转移这些健康状况。
这是《科学》杂志上一篇新的观点文章得出的结论。也许通常被认为是“非传染性”的疾病——比如糖尿病或哮喘,它们没有病毒或细菌在宿主之间传播——实际上是通过肠道微生物在患者之间悄悄传播的。论文合著者、不列颠哥伦比亚大学微生物学家布雷特·芬利(Brett Finlay)说,要获得肠道细菌在人与人之间传播并引发这些疾病的科学证据将很困难。但如果理论是正确的,这将为科学家提供一个全新的疾病研究角度。
我们的肠道充满了数千种细菌,它们帮助我们消化食物、产生营养物质和建立免疫系统。芬利说,基因很少决定我们肠道中生长什么,他的写作得到了加拿大高等研究院(一个支持跨学科研究的非营利组织)的支持。在那里茁壮成长的绝大多数物质来自我们的环境——我们吃什么、我们住在哪、我们如何与周围环境互动。我们与谁互动也很重要,他的文章解释道。配偶比远居的兄弟姐妹共享更多相似的肠道微生物——并且,至少在一个案例中,仅凭微生物组就表明了谁与谁结婚。
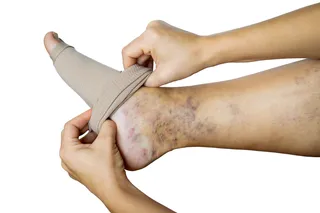
最近的研究甚至发现,随着人们改变他们互动的人,他们会发展出一些传统上的非传染性疾病。例如,驻扎在平均体重指数较高的国家的美国军人家庭,其体重指数也较高;而驻扎在低体重指数国家的家庭,其体重指数较低。生活在印度的人患溃疡性结肠炎的几率很低——但移民到英国、美国或加拿大的人患此病的几率更高。一些研究表明,将健康状况与周围的人融合是生活方式和饮食改变的副产品。
但如果肠道细菌在这些健康状况中起作用,那么人们可能从新朋友那里获得的不仅仅是新知识和食物——也许他们也获得了他们的一些细菌。“考虑到我们所知的一切,这是合理的,”芬利说。“非传染性疾病的最佳预防策略是饮食和运动。那么[饮食和运动]还做什么呢?彻底改变你的微生物。”
目前,这一理论还需要更多的科学证据。芬利说,故意在人类之间传播疑似致病因子是不道德的。但也许证明其反面——将健康人的健康肠道微生物给予病人——可以证实这一理论。芬利还说,区分细菌效应与生活方式和饮食选择效应也将是一个挑战,因为这两者经常同时改变。虽然有证据表明微生物组与II型糖尿病甚至阿尔茨海默病有关,但对于某些疾病,如癌症,这种联系则较弱。
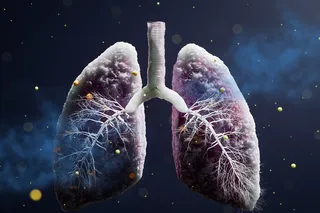
但芬利说,如果我们的肠道细菌能够影响我们周围人的健康,这可能会重塑公共卫生官员追踪和研究疾病的方式。芬利说,在美国目前的主要死亡原因中,只有流感和肺炎明确与微生物有关。如果一些“非传染性疾病”可以通过微生物传播,那么大多数主要死亡原因都将与我们肠道中的微生物有关。