黑猩猩也会感染艾滋病。这是一个重要的发现,但最让我着迷的是它是如何被发现的。这是一个关于两种科学的故事,这两种科学对于深入了解生命都至关重要,但如今却严重失衡。20世纪60年代,简·古道尔(Jane Goodall)进行了早期对野生黑猩猩进行的长期研究。古道尔(Goodall)做出了重要观察,她注意到黑猩猩可能非常合作,但也可能非常暴力,种群之间会发生类似战争的冲突。古道尔(Goodall)的研究是长期以来前往动物所在地并追踪它们多年的传统的一部分。古道尔(Goodall)没有将巨大的实验室设备箱带到坦桑尼亚;相反,她带来了耐心和仔细的观察。当然,进行这类科学研究也存在一些严峻的挑战。野外生物学家通常只能研究相对较少的个体动物,因为它们非常难以找到。小样本量总是使广泛的概括存在风险。野生动物也生活在一个极其复杂的大环境中。它们受到大量变量的影响——天气、食物供应、最新的疫情爆发、最顶层雄性与其年轻竞争者之间最新的争斗。任何时候动物的状态都可能受到其中许多变量的影响,这使得揭示其自然史的重要潜在规律更加困难。而且由于这种科学研究需要很长时间,所以如果只通过科学家发表的论文来了解它,可能会显得微不足道。古道尔(Goodall)的科学与病毒学实验室的科学之间的对比是巨大的。科学家们不仅仅是观察病毒,还可以进行实验来检验假设——进行精确控制的实验。科学家可以对病毒进行基因改造,以发现其基因物质的每一部分是如何(或如何不)帮助它感染宿主的。他们可以仔细选择宿主进行感染,例如比较两组宿主,这两组宿主可能只在一种特定的细胞受体上有所不同。他们可以追踪病毒通过细胞的传播过程,然后再次离开;他们可以像打开一个幸运签语饼一样轻松地对病毒基因进行测序。他们每年都可以发表大量关于他们发现的论文。正如我在PLOS Computational Biology上发表的这篇论文中所写的那样,这两种生物学之间的鸿沟已经存在了几十年。这种鸿沟导致了一些不幸的偏见。自然史有时被视为镀金的蝴蝶收藏。与此同时,基于实验室的分子生物学有时被视为死板和毫无意义的还原主义。但是,一方认为自己可以没有另一方而独立存在,这将是一个错误。了解艾滋病的起源就是一个很好的例子。2007年,全球估计有3300万人感染了艾滋病毒,每年估计有310万人死于与艾滋病相关的疾病。然而,就疾病而言,艾滋病毒是一种后来者。科学家们直到20世纪80年代初才意识到它的存在,当时它还相对罕见,之后迅速成为全球性流行病。科学家们试图通过查阅医疗记录和血液样本来寻找可能被忽视的早期艾滋病毒感染病例。最早的艾滋病毒样本来自1959年在刚果民主共和国首都金沙萨的一名患者血液样本中采集的。艾滋病毒的神秘出现引发了许多关于其来源的猜测——包括声称疫苗接种运动通过被猴子病毒污染的疫苗将其引入人群。但当科学家们重建病毒及其近亲的进化树时,他们就可以驳斥这些说法。
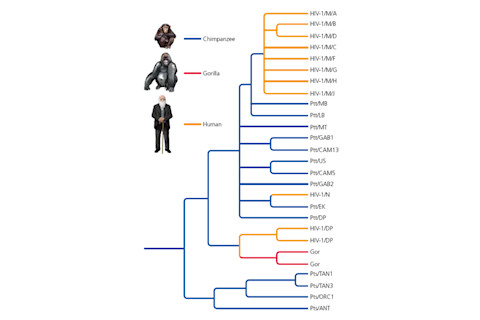
科学家们一发现艾滋病毒,就很清楚它属于一种称为慢病毒的群体。慢病毒是具有表面尖刺小颗粒,它们将基因编码在RNA中。它们感染哺乳动物,如猫、马和灵长类动物,通常侵入某些类型的白细胞。基因研究表明,艾滋病毒与感染猴子和猿类的慢病毒株——即猴免疫缺陷病毒,简称SIV——关系最密切。艾滋病毒实际上并非单一谱系。它是具有不同起源的几种不同菌株。艾滋病毒有两种主要形式,艾滋病毒-1和艾滋病毒-2。艾滋病毒-2相对温和,是由生活在一种称为黑白疣猴的猴子身上的SIV进化而来。艾滋病毒-1的故事,造成了绝大多数艾滋病病例,更为复杂,如这个图表所示。(它来自我即将出版的书《纠缠的银行:进化入门》)。这张图揭示了,它实际上是几种菌株,所有这些菌株都从黑猩猩身上传播而来。科学家们最初是通过观察圈养动物发现黑猩猩身上的SIV。但为了真正了解病毒的多样性,他们不得不离开实验室的舒适环境,前往黑猩猩栖息的地方。野生黑猩猩很难接受抽血,因此科学家们开发了从黑猩猩留下的粪便中提取病毒DNA的方法。但是,为了找到那些黑猩猩的粪便,你必须找到黑猩猩(以及它们过夜的树)。这些研究表明,两个亚种的黑猩猩携带SIV,但艾滋病毒-1只从其中一个亚种进化而来,即生活在非洲西部金沙萨附近的P. troglodytes troglodytes(在此图谱中标注为Ptt)。古道尔(Goodall)在中非黑猩猩Pan troglodytes schweinfurthii(在此图谱中标注为Pts)身上也有自己的SIV。

这些研究表明,SIV进化成艾滋病毒是由于猎人在日益增长的“丛林肉”行业中捕杀猿猴出售。灵长类动物血液中的病毒可能进入了猎人的皮肤伤口,其中一些病毒发生了变异并适应了新的宿主。了解艾滋病毒树的结构,使科学家们能够精确定位这些适应性。例如,事实证明,当艾滋病毒-1的三种菌株都从黑猩猩病毒祖先进化而来时,它们都在同一个蛋白质的相同位置获得了相同的新氨基酸。黑猩猩中的任何SIV菌株都不会产生这种氨基酸。这种突变改变了一个编码病毒外壳的基因,实验表明,这对新艾滋病毒菌株在人类身上的成功至关重要。这种突变可能使病毒能够更好地操纵新宿主来构建自身的副本。当然,艾滋病不仅仅是一种病毒。一旦一个人感染了艾滋病毒,病毒可能需要数年时间才能摧毁他的免疫系统,从而导致各种寄生虫乘虚而入。当科学家们研究感染SIV的圈养黑猩猩时,他们没有看到任何类似艾滋病的情况。这至少是令人好奇的。也许黑猩猩和病毒已经共同进化到和平共处。当艾滋病毒-1传播到人类时,它的进化发生了糟糕的转变。但野外的黑猩猩呢?它们会得艾滋病吗?这是一个非常简短的问题,但花了很长时间才得到答案。一个科学团队在贡贝国家公园简·古道尔(Jane Goodall)的研究基地安顿下来,并利用她数十年的野外工作,对94只黑猩猩进行了长达九年的追踪。他们搜寻黑猩猩粪便中的SIV,然后追踪黑猩猩本身,观察它们的健康状况、后代和寿命。当黑猩猩死亡时,科学家们对其进行尸检,以了解SIV对它们的影响。结果,今天发表在《自然》杂志上,结果令人震惊。在94只黑猩猩中,有17只感染了SIV。感染SIV的黑猩猩的死亡率是非感染黑猩猩的10到16倍。感染的雌性黑猩猩比未感染的生育的更少,而且它们的孩子中没有一个活到一岁。病理学家发现,死亡的感染黑猩猩看起来像是患有艾滋病,其CD4+ T细胞等免疫细胞水平较低,淋巴组织受损。这一发现引出了各种各样的问题。贡贝的黑猩猩确实会生病,但并不像人类感染艾滋病毒-1那样严重。为什么?没有证据表明SIV是从P. t. schweinfurthii传播到人类的。相反,它传播了三次或更多次,是从P. t. troglodytes传播的。据所有人所知,那些黑猩猩并没有患艾滋病。但是,话说回来,还没有人发表过像贡贝黑猩猩那样的研究。这项研究将揭示什么,如果有人进行了的话?P. t. troglodytes是最近感染人类和贡贝黑猩猩的来源吗?而且,对我来说,特别有趣的是,科学家们以前没有注意到黑猩猩的艾滋病。伦敦大学学院的艾滋病毒研究员罗宾·韦斯(Robin Weiss)和剑桥大学的乔纳森·希尼(Jonathan Heeney)在《自然》杂志上发表了一篇评论,他们认为圈养黑猩猩的生活条件人工,保护了它们免受艾滋病的侵害。在现实世界中,黑猩猩面临着各种病原体的攻击,感染可能会激活免疫系统,从而引发病毒的攻击,最终导致艾滋病。换句话说,只有简·古道尔(Jane Goodall)开创的慢炖科学才使科学家们能够发现对一种已成为人类现代史上最毁灭性的瘟疫之一的病毒的最基本的事实之一。慢炖科学将来可能会提供更多线索——但前提是它的价值得到承认,前提是黑猩猩能够克服SIV以及如今威胁它们生存的所有其他威胁。[古道尔(Goodall)图片:简·古道尔(Jane Goodall)的黑猩猩]