17 世纪中期,罗伯特·胡克通过简陋的显微镜观察,引发了一场革命。我们今天对生命体基本结构的理解,始于他检查薄薄的软木片,看到了像僧侣居所一样有间隔的小隔间:他称之为细胞。
几个世纪以来,随后的进步加深了我们对这些结构的理解,现在我们知道它们是生命的基本单位。仅在过去十年里,技术上的飞跃使科学家以前所未有的精度探索了细胞的微观世界。这些发展催生了一个庞大的科学巨头,其规模和重要性可与人类基因组计划媲美。
该项目被称为人类细胞图谱(HCA),是一项国际研究,旨在创建一个全面的三维参考图谱,描绘人体所有器官系统中不同细胞类型及其状态下基因的表达(或激活)情况。该全球联盟包括来自 55 个国家 584 个研究所的 1000 多名科学家。虽然他们不会试图绘制出人体所有 37 万亿个细胞的详细图谱,但初步研究正聚焦于五个主要领域,包括癌症;大脑和神经系统;免疫系统;作为我们全身保护层的上皮组织;以及从子宫内细胞分化开始的人体发育。
这项工作有可能开启精准医疗的新时代,彻底改变我们对健康和疾病的理解,从而更好地检测、监测和治疗困扰人类的疾病。“细胞的多样性远超我们之前的想象,技术的爆炸式发展正揭示这一点,”英国(U.K.)细胞遗传学负责人 Sarah Teichmann 说。
细胞的宇宙
我们的细胞是复杂的生命体。每个细胞都由数百万个分子组成,这些分子不断地相互传递信息,以完成细胞的基本工作,无论该细胞的具体职责是修复组织损伤、清除碎片,还是沿着大脑的神经回路传递信息。每个细胞核内都盘绕着 DNA 的双螺旋结构,两条交织在一起的化学链,上面布满了超过 20000 个基因,提供了生命的基本蓝图。每个基因表达时,都会产生 RNA,然后 RNA 再产生蛋白质,这些蛋白质是细胞中的“主力军”。蛋白质也存在于细胞表面,就像微型潜望镜一样扫描周围环境,寻找食物、危险或外来入侵者。它们将这些信息传递给内部的蛋白质,内部蛋白质利用这些数据重新开始细胞更新和再生的过程,而这一切都始于基因发出的信号。
但尽管每个细胞都携带相同的基因,但每个细胞只使用其中一部分指令,就像一首奏鸣曲只使用了钢琴的部分琴键一样。该联盟的崇高目标是,在对人体 37 万亿个细胞进行分类的过程中,理解每种细胞类型中激活了哪些特定基因——用科学术语来说,就是基因表达的模式。
他们计划破译健康细胞内基因如何正确表达。 Dana Pe’er,该联盟的首席成员之一,也是纽约纪念斯隆凯特琳癌症中心计算与系统生物学项目的负责人,她说,利用这些信息作为参考点,将使他们能够立即发现基因表达偏离正常的地方。她表示,这可以揭示基因何时在错误的时间、错误的细胞类型或错误的数量下被表达。“我们正在研究一系列复杂的问题,”她说。“这些问题包括细胞群如何协同工作来对抗病原体,或者疾病如何导致细胞的调控回路失灵。”
最终,这个由细胞类型、它们的状态、位置和基因表达索引的大型细胞库——可能有助于科学家们取得无数新发现。其中一个更直接的应用是:识别癌症或遗传性疾病(由突变 DNA 引起)等疾病中基因信号为何会出错。研究人员还可以更好地了解脑细胞,以帮助治疗阿尔茨海默病、帕金森病和肌萎缩侧索硬化症等神经退行性疾病。细胞图谱还可能揭示个体患者的基因对哪些药物反应最佳。同样,也可以确定他们的身体可能已经产生耐药性的治疗方法。
这项研究还可以帮助医生知道应该完全避免给患者使用哪些药物。药物往往可能出乎意料地有毒。这是因为治疗可能针对特定的蛋白质,但我们却不知道该蛋白质在身体的另一个部分可能具有有益的功能。“一旦我们有了很好的参考工具,就能很快发现这些问题,” Aviv Regev 说,他是麻省理工学院和哈佛大学博德研究所的计算与系统生物学家,曾牵头创建 HCA,现在共同主持其组织委员会。
细胞冰沙
长期以来,科学家们一直想了解基因的复杂配列如何在每个单独的细胞内发挥魔力,但直到过去十年,技术才跟上。大约在 2012 年,一项名为单细胞基因组学(single-cell genomics)的技术越来越受欢迎,并提供了一种对单个细胞进行分类的新方法。科学家可以从试管中取出单个细胞并测序其遗传信息。但这意味着数十万甚至数百万个细胞未能被测序。为了解决这个问题,科学家们将各种细胞的结果混合在一起,作为整个细胞群的代表——Regev 将这一过程比作制作水果冰沙。
这项技术忽略了个体细胞的变异范围,或者说,用冰沙的比喻来说,未能区分草莓、蓝莓和奇异果的味道。“冰沙制作过程结束时,它可能看起来是粉红色的,”Regev 说。“但如果里面有几个奇异果,你可能就认不出来了。而且我们知道细胞很可能彼此不同——而这些差异很重要,因为它们都反映了细胞可能是什么或将要做什么。”
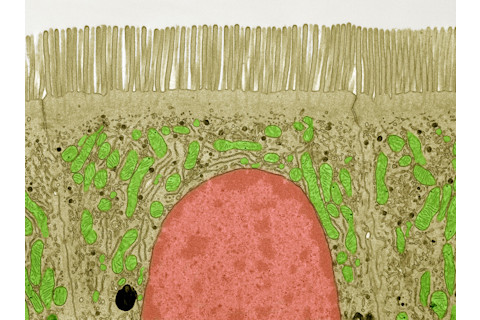
一种上皮细胞。(图片来源:Thomas Deerinck/Science Source)
Thomas Deerinck/Science Source
由于 Regev 参与发明的一项微技术在 2015 年的开发,科学家们现在可以同时测序数千个单独的细胞。这项新技术将每个细胞封装在微小的液滴中。然后,一个过程会将细胞分解,在此过程中,其 RNA 片段被捕获在微小的珠子上进行分析。Teichmann 表示,这导致了一系列发现,揭示了可能存在数千种——而非仅仅数百种——不同的细胞类型。仅在免疫系统中,我们现在就知道有 200 多种细胞类型,即使是覆盖眼球表面的微小视网膜也有大约 100 种不同类型的细胞。
受这些发现的鼓舞,世界各地的科学家们开始谈论深入探究每个细胞并绘制其组成部分图谱的诱人前景。到 2014 年,Regev 开始“宣扬”创建人类细胞图谱的想法,并最终引起了 Teichmann 的兴趣,这促使他们两人都迈出了实际行动的重大一步。
大资助者介入
HCA 已经获得了强大的机构支持,包括来自美国国立卫生研究院(National Institutes of Health)的 2 亿美元以及来自伦敦生物医学研究慈善机构 Wellcome Trust 的约 900 万美元。它还获得了 Chan Zuckerberg Initiative 的 1500 万美元赠款,该机构正在资助开源数据协调平台,该平台将存储研究人员生成的海量数据。
早期成功
HCA 于 2017 年启动,已经取得了一些有趣的发现。2018 年,Regev 和来自博德研究所(Broad Institute)和麻省总医院(Massachusetts General Hospital)的研究人员发现,气管内壁有七种细胞类型——比预期的多一种。这种新型细胞在一种特定基因的表达中尤为重要,该基因突变会导致囊性纤维化,并可能对理解和最终开发出这种遗传病的治疗方法至关重要。这项发现还可以带来更好的哮喘治疗方法。
在另一项 2018 年的研究中,Teichmann 的团队与来自剑桥大学(University of Cambridge)和纽卡斯尔大学(Newcastle University)的合作者一起,对最常见的儿童和成人肾癌背后的癌细胞进行了表征。具体来说,他们发现儿童肾癌细胞出现时,就像它们还在子宫内发育时一样,这表明这些细胞被困在不成熟的胎儿状态。“我们发现了驱动肿瘤的是哪些细胞,”Teichmann 说,“这是一个极其重要的发现。”她认为这可以带来更精准的靶向疗法。
Regev 的团队最近的研究也为一种新型癌症药物——免疫检查点抑制剂(prompt the immune system to attack malignant cells)——为何只对少数患者有效提供了一些线索。在一项研究中,他们考察了黑色素瘤细胞中基因的激活情况,发现有些肿瘤存在一类细胞,它们根本不对免疫疗法作出反应,从而阻止免疫系统细胞攻击癌细胞。研究人员目前正在寻找逆转这种耐药性的方法。Regev 说,现在他们能够深入了解细胞在做什么,“你可以倾听这些不同细胞之间的‘交谈’,以了解哪些信号出错,以及哪些信号阻止了肿瘤生长或恢复了治疗效果。”
HCA 面临着许多技术挑战——仅仅建立一个让所有实验室共享数据的平台就将是一个挑战。但 Regev 毫不畏惧,并预测他们将在十年内拥有完整的图谱。
Linda Marsa是《Discover》杂志的特约编辑。