查看 Carl Zimmer 的新电子书《Brain Cuttings》,可在 Amazon、Barnes and Noble 以及 carlzimmer.com 购买。
本月专栏讲述了两只老鼠的故事。一只老鼠在幼年时得到了母亲的许多关注;她的母亲每天舔它很多次。另一只老鼠的经历则不同。它的母亲几乎不舔它。这两只老鼠长大后,性格截然不同。被忽视的老鼠很容易被噪音吓到。它不愿意探索新地方。当它经历压力时,会产生大量的激素。与此同时,得到母亲更多关注的老鼠则不易受惊吓,更有好奇心,也不会承受压力激素的激增。
同样的道理在许多实验室里已经重复了数百次。老鼠幼年时的经历改变了它们成年后的行为。我们都直觉地认为这对于人类也同样适用,只是将舔毛换成了学校、电视、家庭 troubles 以及孩子们经历的一切。但在这个看似显而易见的生活事实背后,隐藏着一个巨大的谜团。我们的大脑是根据基因编码的“食谱”发育的。我们每个脑细胞都含有我们出生时就拥有的相同基因组,并利用这些基因在其一生中构建蛋白质和其他分子。这些基因中的 DNA 序列几乎是固定的。要让经历产生对我们行为的长久改变,它们必须以某种方式深入我们的大脑,改变这些基因的工作方式。
神经科学家们现在正在绘制这种机制的图谱。看来,我们的经历实际上并不会重写我们大脑中的基因,但它们可以做到几乎同样强大的事情。依附在我们 DNA 上的是成千上万的分子,它们可以关闭一些基因,使另一些基因活跃。我们的经历可以物理地重新排列这些开关的模式,并在此过程中改变我们脑细胞的工作方式。这项研究具有一个非常令人兴奋的意义:我们可能能够自己重新排列这种模式,从而使人们摆脱像严重焦虑和抑郁这样的精神疾病。事实上,科学家们已经在小鼠身上缓解了这些症状。
两大家族分子执行了这种基因调控。一大家族是甲基,由碳和氢组成的分子帽。附着在基因上的一串甲基可以阻止细胞读取其 DNA 序列。结果,细胞就无法从该特定基因产生蛋白质或其他分子。另一大家族由卷曲蛋白组成,这些分子将 DNA 缠绕成线轴。通过收紧线轴,这些蛋白质可以隐藏某些基因;通过放松线轴,它们可以使基因活跃起来。
甲基和卷曲蛋白——科学家们称之为表观基因组——共同构成了大脑得以形成的基础。胚胎最初是一团微小的相同干细胞。随着细胞分裂,它们都继承了相同的基因,但它们的表观遗传标记发生了变化。随着分裂的继续,细胞传递的不仅仅是基因,还有它们对这些基因的表观遗传标记。每个细胞特定的活跃和沉默基因组合有助于决定它将形成何种组织——肝脏、心脏、大脑等等。表观遗传标记非常持久,这就是为什么你醒来时不会发现你的大脑变成了胰腺。
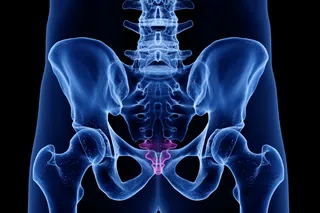
然而,我们的经历可以重写表观遗传密码,这些经历甚至可以在我们出生前就开始。例如,为了建立正确的表观遗传标记模式,胚胎需要从母亲那里获得原材料。一种重要的原料是叶酸,一种存在于许多食物中的营养素。如果母亲摄入的叶酸不足,她们未出生的孩子可能会形成受损的表观遗传标记模式,导致基因功能异常。这些错误的标记可能导致脊柱裂,一种脊柱未能完全形成的疾病。
其他化学物质也会干扰胚胎中的表观遗传标记。去年,印第安纳大学的Feng C. Zhou发现,当怀孕的实验鼠摄入大量酒精时,它们胚胎上的表观遗传标记会发生剧烈变化。结果,它们大脑中的基因以异常模式开启和关闭。Zhou 认为,这种表观遗传密码的重写是导致胎儿酒精综合征毁灭性症状的原因,该综合征与低智商和行为问题有关。
即使在出生后,大脑中的表观遗传标记也可以改变。在过去的十年里,麦吉尔大学的神经生物学家Michael Meaney及其同事一直在进行一项关于经历如何重编程大脑基因的最详细的研究之一。他们正在揭示两只老鼠故事的分子基础。
得到大量舔舐的老鼠与得到少量舔舐的老鼠之间的差异并非源于基因差异。Meaney 在一项涉及新生仔鼠的实验中发现了这一点。他将母亲舔舐很少的仔鼠放在喜欢舔舐的寄养母亲那里,反之亦然。仔鼠与寄养母亲的经历——而不是它们从亲生母亲那里继承的基因——决定了它们成年后的个性。
为了弄清楚舔舐是如何改变老鼠的,Meaney 及其同事仔细检查了动物的大脑。他们在老鼠的海马体中发现了重大差异,海马体是大脑中负责组织记忆的部分。海马体中的神经元通过制造特殊的受体来调节对压力激素的反应。当受体抓住激素时,神经元通过泵出触发一系列反应的蛋白质来做出反应。这些反应在大脑中传播,并到达肾上腺,对压力激素的产生起到制动作用。
然而,为了制造激素受体,海马体必须首先接收信号。这些信号会开启一系列基因,最终导致海马体中的神经元构建受体。Meaney 及其同事在一种被称为糖皮质激素受体基因的基因中发现了一些不寻常之处:与舔舐很少的老鼠相比,得到大量舔舐的老鼠中,这个基因的开关 DNA 区域是不同的。在舔舐很少的老鼠中,糖皮质激素受体基因的开关被甲基帽封住,而舔舐不足的老鼠的神经元产生的受体数量较少。因此,海马体神经元对压力激素的敏感性较低,也较难抑制动物的压力反应。结果,舔舐不足的老鼠长期处于压力之下。
这些研究暗示了青年时期的经历如何重写我们大脑中的表观遗传标记,从而改变我们成年后的行为。当然,Meaney 及其同事无法通过对人类进行类似实验来检验这一假设,但去年他们发表了一项研究,非常接近。
Meaney 的团队检查了 36 具尸体大脑。其中 12 具大脑来自有童年虐待史的自杀者。另外 12 人自杀,但没有此类历史。最后 12 人死于自然原因。科学家们重点研究了尸体海马体的细胞,检查了他们在老鼠身上研究过的压力激素基因的开关。Meaney 及其同事发现,遭受过儿童虐待的人的大脑,开关上的甲基比其他人群要多,这与在幼年舔舐很少的老鼠中观察到的情况一致。正如那些老鼠产生的压力激素受体较少一样,遭受过儿童虐待的人的神经元受体也较少。
儿童虐待可能像父母的忽视影响幼鼠一样,在受害者身上留下印记。虐待似乎改变了他们海马体的表观遗传标记。结果,他们的神经元产生的压力受体较少,导致他们无法调节压力激素,从而一生都处于焦虑状态。过度的压力可能导致了他们的自杀。
海马体可能不是唯一一个经历重写大脑表观遗传标记的地方。最近,一个国际研究小组比较了 44 名自杀者和 33 名死于自然原因的人的大脑。科学家们研究了一个产生 BDNF 蛋白的基因,该蛋白在大脑的 Wernicke 区促进激素受体的产生。这个区域位于大多数人左耳后面,帮助我们理解词义。今年三月,研究人员报告说,在自杀者的 Wernicke 区,BDNF 开关上的甲基比其他人的多。
环境的影响并非止于童年。最近的研究表明,成年人的经历也可以重新排列大脑中的表观遗传标记,从而改变我们的行为。例如,抑郁症在很多方面可能是一种表观遗传疾病。几组科学家通过让小鼠互相搏斗来模仿人类抑郁症。如果一只小鼠在一系列对抗占主导地位的对手的战斗中失败,它的性格就会改变。它会回避与其他老鼠接触,并且活动减少。当老鼠可以使用一台机器给自己注射可卡因时,失败的老鼠会摄入更多。
纽约市西奈山医学院的神经科学家 Eric Nestler 想知道这些抑郁小鼠的大脑是什么样的。去年秋天,他报告发现了一个名为伏隔核的脑区的重大差异。抑郁症改变了这个区域可能不是巧合,因为伏隔核在大脑的奖励系统中起着重要作用,帮助我们确定事物的价值以及我们从中获得的愉悦感。
Nestler 及其同事在伏隔核中发现的变化是表观遗传的:那些区域神经元中的一些 DNA 在抑郁小鼠中缠绕得更紧或更松。这种表观遗传改变可能会永久性地改变那些小鼠大脑中哪些基因是活跃的。这可能也适用于人类。Nestler 的团队检查了生前被诊断患有抑郁症的人的尸体大脑。他们在人类伏隔核中发现了相同的表观遗传改变。
如果科学家们能够查明我们的经历所赋予的表观遗传改变,那么就有可能逆转这些改变。Nestler 及其同事将一种称为HDAC 抑制剂的药物注入了他们抑郁小鼠的伏隔核。这些药物可以松开紧绷的 DNA 线轴,使细胞能够重新访问基因。治疗十天后,这些小鼠更愿意接近其他小鼠。该药物还消除了动物身上抑郁症的许多其他症状。
我们可以重写我们大脑中的表观遗传密码的可能性可能令人兴奋,但也令人望而生畏。修改表观遗传标记并不容易——这是一件好事。毕竟,如果我们的甲基和卷曲蛋白不断变化,抑郁症将是最小的问题。没有什么比发现你的大脑变成了胰腺更糟糕的了。