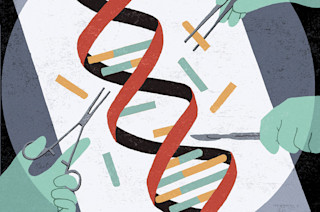
如今,研究人员使用 CRISPR 进行基因编辑时,他们的系统会先将 DNA 链切断,然后插入新基因,并利用细胞自身的修复机制将 DNA 链重新连接起来。
这项技术总体上效果很好,但可能导致错误,并且成功率因细胞类型而异。多年来,科学家们一直在寻找 CRISPR 的改进版本。
现在,来自哈佛大学和麻省理工学院博德研究所的研究人员发现了一种新的蛋白质,可以在不先切断 DNA 的情况下将定制基因插入 DNA。该团队表示,这一发现有助于使未来的基因编辑工作更安全、更高效,尽管还需要进一步研究才能将该系统应用于人类。
更优的编辑
目前已有几种 CRISPR 系统的变体,但传统上,CRISPR 是利用细菌抵抗病毒的天然防御机制。细菌自然会从感染病毒的 RNA 中提取一小段 RNA,并将其整合到自己的基因组中,以便记住病毒并防止将来再次感染。它们用来做到这一点的系统在成为基因编辑工具之前就已经被称为 CRISPR。
但在 2012 年,研究人员 Jennifer Doudna 和 Emmanuelle Charpentier 开发了一种名为 Cas9 的 CRISPR 蛋白质版本,可以编程在基因组的特定位点切割和插入基因。这构成了我们在过去几年中看到的 CRISPR 研究 爆炸式发展 的基础。
然而,Cas9 版本的系统有时会产生所谓的“脱靶”效应,在基因组中错误的位置进行切割。科学家们一直在争论这种故障的风险有多大,但无论如何,它始终存在风险。
新的 CRISPR 系统,于周四发表在Science杂志上,基于一种遗传怪癖,有望完全绕过脱靶切割问题。这种新方法被称为 CRISPR 相关转座酶 (CAST),它不像 CRISPR 那样需要切断双链 DNA 来完成工作,而是直接插入基因,无需进行双链切割。
无需切割的 CRISPR
这项进展来自一个团队,其中包括博德研究所和麻省理工学院麦戈文研究所的 Feng Zhang,他是 CRISPR 的共同发现者之一。他们的灵感来自一种称为转座子(也称为“跳跃基因”)的基因。这个名字很贴切,因为转座子可以在我们的基因组中移动,改变它们在我们基因蓝图的 DNA 链中的位置。
这可能是有益的,因为转座子有助于修复突变,但在某些情况下也可能有害,因为失控的跳跃基因可能会导致自身的有害突变。然而,对 CRISPR 研究人员来说,关键在于转座子能够插入我们的 DNA 而不破坏它。
他们从两种细菌 *Scytonema hofmanni* 和 *Anabaena cylindrica* 中提取了能够使基因插入基因组的转座酶。研究人员将该蛋白质与一种称为 Cas12k 的 CRISPR 相关酶结合,Cas12k 可以将其引导至基因应插入基因组的精确位置。
研究人员在 *大肠杆菌* 中测试了他们的 CAST 系统,他们表示该系统既精确又高效,并且优于现有的 CRISPR 技术。尽管新技术尚未在细菌以外的生物体中进行测试,但它有望为新一代更智能、更高效的基因编辑系统带来希望。